Сумесная даследчая група з Гарвардскай медыцынскай школы (HMS) і Генеральнай бальніцы Масачусецкага тэхналагічнага інстытута заяўляе, што ім удалося рэгуляваць магутнасць мікрадыскавага лазера з дапамогай метаду травлення PEC, што робіць новую крыніцу для нанафатонікі і біямедыцыны «перспектыўнай».
(Магутнасць мікрадыскавага лазера можна рэгуляваць метадам травлення PEC)
У паляхнанафатонікаі біямедыцына, мікрадысклазерыі нанадыскавыя лазеры сталі перспектыўнымікрыніцы святлаі зонды. У некалькіх сферах прымянення, такіх як фатонная сувязь на чыпе, біявізуалізацыя на чыпе, біяхімічнае датчыцтва і апрацоўка квантавай фатоннай інфармацыі, ім неабходна дасягнуць лазернай магутнасці пры вызначэнні даўжыні хвалі і дакладнасці ультравузкага дыяпазону. Аднак вытворчасць мікрадыскавых і нанадыскавых лазераў з такой дакладнай даўжынёй хвалі ў вялікіх маштабах застаецца складанай задачай. Сучасныя працэсы нанавытворчасці ўводзяць выпадковасць дыяметра дыска, што ўскладняе атрыманне зададзенай даўжыні хвалі пры лазернай апрацоўцы і вытворчасці масы. Цяпер каманда даследчыкаў з Гарвардскай медыцынскай школы і Цэнтра Уэлмана пры Масачусецкай агульнай бальніцы...Оптаэлектронная медыцынараспрацавалі інавацыйную тэхніку оптахімічнага (ПХТ) травлення, якая дапамагае дакладна наладзіць даўжыню хвалі лазернага выпраменьвання мікрадыскавага лазера з субнанаметравай дакладнасцю. Праца апублікавана ў часопісе Advanced Photonics.
Фотахімічнае травленне
Паводле паведамленняў, новы метад каманды дазваляе вырабляць мікрадыскавыя лазеры і нанадыскавыя лазерныя масівы з дакладнымі, загадзя вызначанымі даўжынямі хваль выпраменьвання. Ключом да гэтага прарыву з'яўляецца выкарыстанне PEC-траўлення, якое забяспечвае эфектыўны і маштабуемы спосаб тонкай налады даўжыні хвалі мікрадыскавага лазера. У вышэйзгаданых выніках каманда паспяхова атрымала мікрадыскі з фасфатавання арсеніду індыя-галію, пакрытыя дыяксідам крэмнія на калоннай структуры з фасфіду індыя. Затым яны дакладна наладзілі даўжыню хвалі лазера гэтых мікрадыскаў да пэўнага значэння, выканаўшы фотахімічнае траўленне ў разведзеным растворы сернай кіслаты.
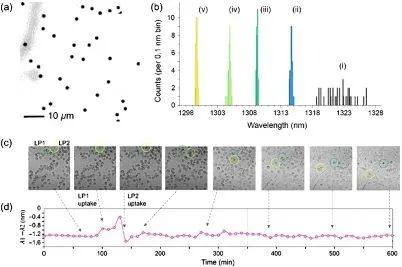
Яны таксама даследавалі механізмы і дынаміку спецыфічнага фотахімічнага (ФЭХ) травлення. Нарэшце, яны перанеслі масіў мікрадыскаў з рэгуляванай даўжынёй хвалі на падкладку з полідыметылсілоксану, каб атрымаць незалежныя, ізаляваныя лазерныя часціцы з рознымі даўжынямі хваль лазера. Атрыманы мікрадыск дэманструе звышшырокапалосную прапускную здольнасць лазернага выпраменьвання, прычымлазерна калонцы менш за 0,6 нм і ізаляваная часціца менш за 1,5 нм.
Адкрыццё дзвярэй для біямедыцынскіх прымяненняў
Гэты вынік адкрывае дзверы для многіх новых нанафатонічных і біямедыцынскіх ужыванняў. Напрыклад, асобныя мікрадыскавыя лазеры могуць служыць фізіка-аптычнымі штрых-кодамі для гетэрагенных біялагічных узораў, што дазваляе маркіраваць пэўныя тыпы клетак і накіроўваць пэўныя малекулы ў мультыплексным аналізе. Маркіроўка, спецыфічная для тыпу клетак, у цяперашні час праводзіцца з выкарыстаннем традыцыйных біямаркераў, такіх як арганічныя флуарафоры, квантавыя кропкі і флуарэсцэнтныя шарыкі, якія маюць шырокую шырыню ліній выпраменьвання. Такім чынам, адначасова можна маркіраваць толькі некалькі пэўных тыпаў клетак. Наадварот, ультравузкапалоснае выпраменьванне святла мікрадыскавага лазера зможа ідэнтыфікаваць больш тыпаў клетак адначасова.
Каманда пратэставала і паспяхова прадэманстравала дакладна настроеныя лазерныя часціцы мікрадыскаў у якасці біямаркераў, выкарыстоўваючы іх для маркіроўкі культываваных нармальных эпітэліяльных клетак малочнай залозы MCF10A. Дзякуючы свайму звышшырокапалоснаму выпраменьванню гэтыя лазеры могуць патэнцыйна зрабіць рэвалюцыю ў біясенсарыцы, выкарыстоўваючы правераныя біямедыцынскія і аптычныя метады, такія як цытадынамічная візуалізацыя, праточная цытаметрыя і мультыомны аналіз. Тэхналогія, заснаваная на травленні PEC, з'яўляецца значным крокам наперад у галіне мікрадыскавых лазераў. Маштабаванасць метаду, а таксама яго субнанаметрычная дакладнасць адкрываюць новыя магчымасці для шматлікіх ужыванняў лазераў у нанафатоніцы і біямедыцынскіх прыладах, а таксама для штрых-кодаў для пэўных папуляцый клетак і аналітычных малекул.
Час публікацыі: 29 студзеня 2024 г.





